美國保健食品相關輔導服務
美國保健食品宣稱怎麼寫才不違規?保健食品該做完那些動作,才能保障合法?
背景
在美國,保健食品並沒有「FDA認證」制度,但這不代表可以自由標示。通常您會碰上這樣的困擾:- 同樣產品,別人可以販售,你卻被扣關?
- 包裝設計完成後,才發現宣稱不能使用?
- 已上市產品,被要求修改或下架?
- 平台接受產品上架,但卻又把我停權?
全球保健食品市場準入策略(美國 / 歐盟 / 中國大陸 / 東南亞 / 紐澳)一次看懂
宣稱若寫錯,可能導致產品下架、扣關或被訴訟。本文說明在美國保健品的合規核心,以及如何委託送件Structure/Function Claim、30天通報要求與常見違規情境,協助評估產品是否具備合規上市條件。
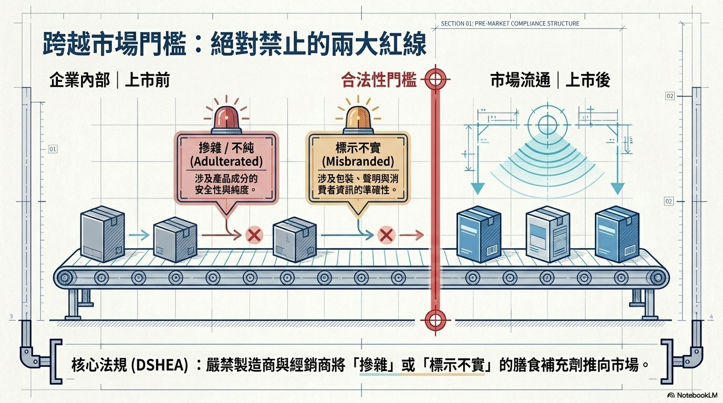
保健食品/機能性食品全球流行,過去美國FDA未嚴格執行灰色地帶的[保健食品]宣稱的管理,美國FDA局長Scott Gottlieb於2019.2.11公開宣布將對市面上各種保健食品加強監管。該局警告,保健食品爆炸性成長,未列明成分、功效誇大不實或誤導情事頻傳,為消費者帶來風險。因此,DIETARY SUPPLEMENT FOOD與一般食品標籤採分流管理,FDA針對宣稱中符合結構式機能宣稱(Structure/functional claim notification)原則者,已有相關規範可以遵循。並且必須於產品上市前30天送件備案。完成後,可以用作產品標示與產品宣傳使用。其他除了要通報的Structure/Function Claim之外,FDA宣稱分類當中,還有Nutrient Deficiency Claim,符合定義者,可以用,但要符合其規定條件;General Well-being符合定義者,可以用,但很不容易被理解;最後是Disease Claim,一定不可以用。這些宣稱的檢查與評估,涉及文化與專業,建議由有經驗的專家評估,以歐美的文化,不會有具體的完全禁用與完全準用。另外還有兩類宣稱,合格健康宣稱(Qualified health claims)與核准的健康宣稱 (Authorized Health Claims),通常由原料商提出申請,讓所有使用該原料的食品可以使用該宣稱,經過FDA不同程度的審核機制後可以使用。
執行的好處
- 在符合FDA規範下提高產品附加價值,合法呈現產品功能。
- 提高DIETARY SUPPLEMENT FOOD廠商輸美商機,增加消費者關注。
服務的模式
保健品產品本身則需要:
- [輸美食品宣稱備案]-結構式機能宣稱通報服務(Structure/functional claim notification) 或 合格的健康宣稱申請服務(Qualified health claims)/核准的健康宣稱申請服務(Authorized Health Claims)後面兩項通常費時較久,需投入較高資源。
- 美國FDA膳食補充劑-合規服務
流程如下:
- 委託者提供配方成分COA與包裝標籤/行銷宣稱
- 委託預審評估宣稱與成分
- 確認成分可用
- 針對宣稱符合定義,分別依宣稱是否需要,而向FDA提出claim notification,並獲得FDA回覆或向FDA申辦核准特定宣稱。
- 並針對產品管理原則,確認對應之產品檢查是否完備。
另外,生產廠商與品牌製造廠,還有下列兩個及格線與加分項的需要:
- 及格線(一定要):輸美食品設施註冊FFR-Food Facility Registration
- 加分項(脫穎而出,提高競爭力):NSF 保健食品相關輔導服務
實例解說
H公司一支含有葡萄糖胺(glucosamine)的膳食補充劑產品,針對關節舒適的宣稱(Joint mobility and comfort,Supports joint strength and flexibility),因成分及宣稱皆符合規範,向FDA通報後,依審查時間(不超過30天)後獲得FDA官網註記備案(註記為final)。則此產品,可以合法標示上述宣稱,並可以在平台上做廣告。您想知道還有哪些宣稱可以,照這樣進行的嗎? 多數宣稱問題,無法透過單一條文判斷。若您已有產品或標示規劃,建議先確認宣稱是否具備合規性,再進行上市。
您想知道還有哪些宣稱可以,照這樣規畫進行,完美通關、保持在店商貨架上不被任意停權的嗎? 多數成分與宣稱問題,無法透過單一條文判斷。若您已有產品或標示規劃,建議先確認宣稱是否具備合規性,再進行上市。