輸入膠囊錠狀食品查驗登記不予登記之原因
2014/04/17
回新聞列表
101年12月至102年11月份完成之「輸入膠囊錠狀食品查驗登記」審查案件中,不予登記之原因以「文件不一致」比率最高,佔26.0%,其次為「逾期未補件」,佔20.5%,再其次為「添加物問題」,佔17.7%。
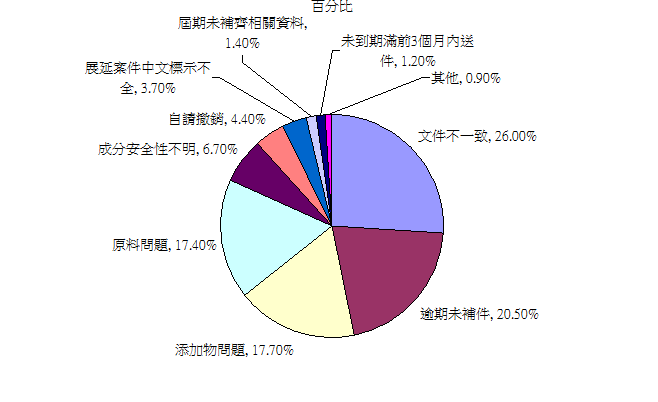
項目說明:
1.文件不一致:案件內所提供之各項文件內容,因列載產品成分、產品外觀色澤、產品總重量或成分添加量等不一致,該等文件無法據予憑辦者屬之。
2.逾期未補件:補件時間已過仍未補附相關資料。
3.添加物問題:案件內使用添加物成分,因其使用範圍、限量等不符「食品添加物使用範圍及限量暨規格標準」之規定者屬之。
4.原料問題:案件內使用原料成分,因其品種、使用部位、加工方法或使用限制等不符「可供食品使用原料一覽表」之規範者屬之。
5.成分安全性不明:案件內使用成分,因未經衛生署評估核定得供食品原料(未收載於「可供食品使用原料一覽表」及「食品添加物使用範圍及限量暨規格標準」中),故在其長期食用安全性未明前,不得供食品加工用者屬之。
6.展延案件中文標示不全:市售產品未標示「食品」、「多食無益」字樣。
7.屆期未補齊相關資料:補件時間已屆滿,惟相關資料未補齊全。
8.未到期滿前3個月內送件:展延案提早送件(未依規定於許可文件有效期限前3個月內辦理展延)。