医疗器械_产业服务

产业资讯
医疗器械产业是一先进国家与开发中崛起国家争先投入的产业,其成长动能来自于各国老年人口数目提升及慢性疾病问题逐渐增加的人口变化因素,也是俗称的健康商机,从产业趋势来看,由于生技相关技术的突破与进化,让生医材料的应用范围逐渐扩增,加上ICT技术的结合,也提供许多创新医疗器械的产生。产业中产品类别之产值规模为心血管相关医材排名第一,其次依序为整形外科相关医材、药物输送相关医材、辅助类相关医材等,B2B业务用(医疗院所)市场稳健成长,虽有些地区市场因健保或福利政策财务扩大问题会有成长沿滞现象出现,反是新兴国家因中产阶级崛起,业务用市场成长快速,一般此区块是以依照医疗科别区分医材的分类,但值得注意的是居家医材的B2C,则随着白色生技概念而快速成长,值得投入,这个区块则以非侵入式的医疗器械类产品居多。
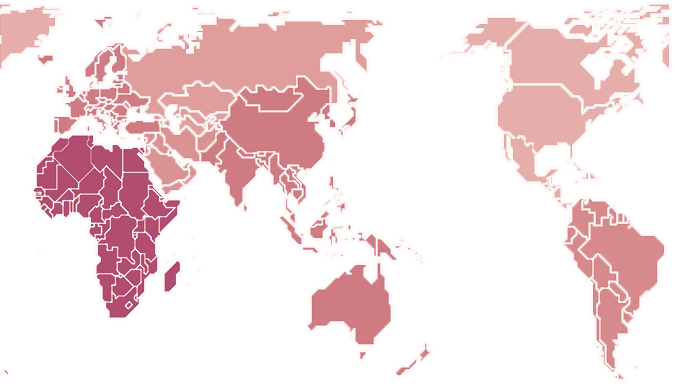
全球医疗器械市场达3,500亿美元,其中生医材料之全球市场规模达500亿美元。美国仍为全球第一大市场约40%;欧盟为第二大区域市场约30%(以德英法为主);亚太成为第三大区域市场约20%(以日韩/大陆为主),如大陆市场产业规模达3,000亿人民币;台湾本身也有800亿元新台币的规模。
从商机面来看,目前诊断设备(或快速诊断技术)需求最大,尤其是体外诊断IVD,可与健康检查挂勾,其次是与牙/骨/眼/慢性病等挂勾的医材,而台湾目前出口的主要类别的则是轮椅类。
进入一个新市场前,您必须首先釐清该市场的产业现况,就可以採用当地第三方委託的特定产业调查服务,委託与自己进行的差别在于,从组织外的角度,更能看清利基市场,不会被过去的经验限制,更可利用产品竞争力分析服务去了解该市场的竞争者现况与其技术水准,也应该利用专利佈局分析服务了解该市场是否有专利限制。其次应该釐清该市场的法规规范,因为医材产品各国都有注册登记的要求,尤其是美国及欧盟市场都有法定代理人的要求。
研发
在产品开发期间,可能会碰到许多规格设计的评估,牵涉后续终产品的安全评估,当发生疑义时,可以採取法规顾问谘询服务的方式(service@e-sinew.com),或专案委託取得评估报告(service@e-sinew.com)。
以主要市场来说,美国FDA法规仍居全球领导地位,但其法规申办时程(约10个月) 较欧盟申办时程长(如英国约5个月),但欧盟法规规范较细(如医材申报分级有6个等级)。
![]() 如果您在开发的过程,发现缺少某一特定关键技术,您可以透过技术交易,经由枢纽技交网来取得,也可以经由商标佈局分析服务、专利佈局分析服务与Know-how佈局来决定研究开发的方向。
如果您在开发的过程,发现缺少某一特定关键技术,您可以透过技术交易,经由枢纽技交网来取得,也可以经由商标佈局分析服务、专利佈局分析服务与Know-how佈局来决定研究开发的方向。
或者您开发出来的成果,也可以思考不走传统产品供应链思维模式(自创品牌各国市场打仗),改为思考智财供应链思维模式,透过枢纽技交网交易取得授权金,授权各国厂商去打仗我们只提供子弹(智财),如果您无法判定您的智财价值,也可以透过智财评价与智财鑑价来得到答案。
组织内部研发很重要的命脉还有
一、知识管理: 知识分享环境塑造、知识文件管理、知识管理流程、知识管理系统导入辅导
二、智财管理: 智慧财产(权)管理系统(TIPS)导入辅导、智慧财产盘点辅导与营业秘密管理制度导入辅导
三、研发制度: 创意管理制度导入辅导、 研发管理制度导入辅导
上市与产品生命週期
任何产品上市后,都可能碰到消费者(或客户)的抱怨问题,且欧美法规都规范要求业者有上市后警戒监督(vigilance)的任务,尤其是抱怨是提给主管当局时,当局是通知法定代理人(非代理商),因此要有Legal Agent(美国)及Authorized Representative(欧盟)维持与当局的沟通。
产品生命週期管理也是上市后,行销的重要任务,在台湾可以与公协会合作,如台湾健康产业协会就是一种选项,其他包括网路行销则应考量SEO之企业网站、网路活动设计与商品设计等作为。
如果在上市时,希望在合法的范围内,进行最恰当的产品包装行销宣传,也欢迎委託产品合法之包装设计。